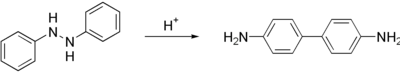Bencidina , la enciclopedia libre
| Bencidina | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 1,1'-biphenyl-4,4'-diamine | ||
| General | ||
| Otros nombres | Benzidine • di-phenylamine • diphenylamine • 4.4'-bianiline • 4.4'-biphenyldiamine • 4.4'-diaminobiphenyl • p-diaminodiphenyl | |
| Fórmula estructural |  | |
| Fórmula molecular | C12H12N2 | |
| Identificadores | ||
| Número CAS | 92-87-5[1] | |
| Número RTECS | DC9625000 | |
| ChEBI | 80495 | |
| ChEMBL | CHEMBL15901 | |
| ChemSpider | 6844 | |
| PubChem | 7111 | |
| UNII | 2X02101HVF | |
| KEGG | C16444 | |
| C1=CC(=CC=C1C2=CC=C(C=C2)N)N | ||
| Propiedades físicas | ||
| Densidad | 1250 kg/m³; 1,25 g/cm³ | |
| Masa molar | 184,1 g/mol | |
| Punto de fusión | 400 °C (673 K) | |
| Punto de ebullición | 0,94 °C (274 K) | |
| Propiedades químicas | ||
| log P | 1.34 | |
| Peligrosidad | ||
| SGA |    | |
| Riesgos | ||
| Riesgos principales | carcinogénico | |
| Compuestos relacionados | ||
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La bencidina es un producto manufacturado que no se encuentra naturalmente en el medio ambiente. Es un sólido cristalino de color amarillo grisáceo, blanco o rojo grisáceo. La bencidina se usó para producir tinturas para telas, papel y cuero. Actualmente no se produce o usa comercialmente en Estados Unidos.[2] Una reacción muy peculiar que presenta es la Transposición bencidínica, una reacción orgánica clásica:
La conversión está descrita como una transposición [5,5] sigmatrópica.[3][4]
Referencias
[editar]- ↑ Número CAS
- ↑ «ATSDR en Español - ToxFAQs™: Bencidina: Departamento de Salud y Servicios Humanos de EE.UU.».
- ↑ H. J. Shine, H. Zmuda, K. H. Kwart, A. G. Horgan, C. Collins, B. E. Maxwell: Mechanism of the benzidine rearrangement. Kinetic isotope effects and transition states. Evidence for concerted rearrangement, in: J. Am. Chem. Soc. 1981, 103, 955–956; doi 10.1021/ja00394a047.
- ↑ H. J. Shine, H. Zmuda, K. H. Kwart, A. G. Horgan, M. Brechbiel: Benzidine rearrangements. 16. The use of heavy-atom kinetic isotope effects in solving the mechanism of the acid-catalyzed rearrangement of hydrazobenzene. The concerted pathway to benzidine and the nonconcerted pathway to diphenyline, in: J. Am. Chem. Soc. 1982, 104, 2501–2509; doi 10.1021/ja00373a028


 French
French Deutsch
Deutsch