Retinoblastoma , la enciclopedia libre
| Retinoblastoma | ||
|---|---|---|
 Tumores del retinoblastoma tomados con un "retinoscan" antes y durante la quimioterapia. | ||
| Especialidad | oncología | |

El retinoblastoma es un tumor canceroso que se desarrolla en la retina causado por una mutación en la proteína Rb, codificada por un gen supresor tumoral denominado RB1.[1] Este tumor se presenta en mayor parte en niños pequeños y representa el 3% de los cánceres padecidos por menores de quince años. Constituye la primera causa de malignidad intra-ocular primaria en los niños y la incidencia anual estimada es de aproximadamente 4 por cada millón de niños.[2]
El mal puede ser hereditario o no serlo. La forma heredada puede presentarse en uno o ambos ojos y, generalmente, afecta a los niños más pequeños. El retinoblastoma presente solo en un ojo no siempre es hereditario. Cuando la enfermedad se presenta en ambos ojos, es siempre hereditaria. Debido al factor hereditario, los pacientes y sus hermanos deben someterse a examen periódicamente, incluyendo terapia genética, para determinar el riesgo que tienen de desarrollar el cáncer.
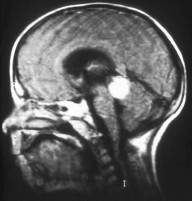
El retinoblastoma tiende a extenderse hacia el cerebro y la médula ósea, y más raramente se disemina por los pulmones. Estos son factores de pronóstico adverso, así como la invasión coroidal y a través del nervio óptico.[1]


Patología
[editar]El retinoblastoma es hereditario en el 40% de los casos; estos niños heredan un alelo mutado (primer evento o hit) en el locus retinoblastoma (RB1) a través de las células germinales. Una mutación somática o cualquier otra alteración en una única célula de la retina da lugar a la pérdida de la función del alelo normal restante, lo que inicia el desarrollo de un tumor. Este trastorno se hereda de manera dominante debido a la presencia de un elevado número de retinoblastos primordiales y su rápida tasa de proliferación, lo cual hace que sea muy probable que se produzca una mutación somática (segundo hit) en uno o más de los retinoblastos existentes. Dado que las posibilidades del segundo evento en la forma hereditaria son tan elevadas, este evento ocurre con frecuencia en más de una célula, de manera que los heterocigotos para esta enfermedad sufren a menudo tumores múltiples que afectan a ambos ojos. Por otro lado, la aparición del segundo evento es un fenómeno de tipo casual y no ocurre en todos los casos; por lo tanto, la penetrancia del gen del retinoblastoma es elevada aunque incompleta. Debido a que la mutación somática del segundo alelo que produce la pérdida de función ocurre con alta frecuencia, las familias que segregan un alelo mutado de un gen supresor de tumores (como RB1) presentan una herencia autosómica dominante de la predisposición al cáncer.[3]
El 60% restante de los casos es de carácter esporádico (no hereditario), en este caso ambos alelos RB1 de una célula han sido inactivados de forma independiente. En estos casos, generalmente el retinoblastoma solo se localiza en un ojo. Una diferencia entre los tumores hereditarios y esporádicos es el hecho de que la edad promedio de los pacientes cuando se inicia la forma esporádica pertenece a la primera niñez, es decir, más tarde que la de los lactantes con la forma hereditaria.
Por tanto, existen dos formas de retinoblastoma: una forma bilateral (en la que aparecen tumores independientes en los dos ojos), familiar, y una forma unilateral (en la que aparece un solo tumor en uno de los ojos), esporádica.[4] Los afectados con el primer tipo tienen una probabilidad 6 veces mayor de desarrollar otros tipos de cáncer durante su vida, sobre todo osteosarcoma.[5] Esto se debe a que en las formas familiares, todos los tejidos somáticos presentan un alelo mutado, por lo que solo necesitan una segunda mutación para provocar la pérdida de función, mientras que en los casos esporádicos hacen falta dos eventos en cada tejido, lo cual ocurre con menor frecuencia. La pérdida de un alelo se puede producir de diversas maneras:[6]
- pérdida del cromosoma 13 completo;
- pérdida del cromosoma 13 normal y duplicación del 13 con el gen mutado;
- recombinación homóloga entre los dos cromosomas 13 durante meiosis;
- adquisición de una mutación independiente en el segundo alelo de RB1;
En todos los casos, excepto en la mutación independiente, se perderían además todos los marcadores genéticos localizados alrededor de RB1 (y por tanto, ligados a este gen), una situación que se denomina pérdida de heterocigosidad (LOH por sus siglas en inglés, lost of heterozigosity).
Un estudio estadístico realizado por el Dr. Alfred G. Knudson y por el Dr. Thaddeus P. Dryja [1] de los casos de retinoblastoma, para explicar precisamente el mecanismo hereditario de este tumor,[7][6] permitió definir el modelo de funcionamiento de los genes supresores de tumores e identificar el primero de estos genes, RB1. Knudson ganó el Premio Albert Lasker a la investigación médica por este trabajo.
Clínica
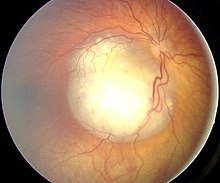
[editar]Uno de los hallazgos más característicos es la leucocoria; de hecho, es la segunda causa más frecuente de leucocoria en niños tras la catarata congénita. También se presenta estrabismo por afectación del área macular, inflamación del segmento anterior, glaucoma, desprendimiento exudativo de retina y proptosis cuando afecta órbita.
Tratamiento
[editar]
La elección de tratamiento que haga el paciente dependerá de cuánto se extienda el mal dentro del ojo y más allá de este.[1] El tratamiento de elección es la cirugía, aunque otras opciones de tratamiento con quimioterapia, termo o crioterapia. En un intento de preservar la visión el ojo menos afectado puede tratarse con radioterapia.
En los últimos años se ha ido desarrollando una técnica conocida como quimioterapia intraarterial supraselectiva que se está extendiendo por todo el mundo debido a sus buenos resultados, su disminución de los efectos secundarios y la mejora en la calidad de vida de los pacientes. Dicha técnica consiste en la introducción de un microcatéter desde la femoral hasta la propia arteria oftálmica, lo que permite aplicar una quimioterapia localizada. De este modo se evitan las repercusiones sistémicas de la quimioterapia tradicional, y además se pueden aumentar las dosis del fármaco quimioterápico hasta niveles que serían mortales si se diesen por vía sistémica.[8][9]
Véase también
[editar]Referencias
[editar]- ↑ a b c Kumar, MBBS, MD, FRCPath, V.; Abul K. Abbas, MBBS, Nelson Fausto, MD and Jon Aster, MD (2009). «Retina and vitreous». En Saunders (Elsevier), ed. Robbins & Cotran Pathologic Basis of Disease (8th edición).
- ↑ «ACS :: What Are The Key Statistics for Retinoblastoma?». web.archive.org. 15 de diciembre de 2004. Archivado desde el original el 15 de diciembre de 2004. Consultado el 10 de agosto de 2020.
- ↑ Nussbaum, R.L.; R. R. McInnes, H. F. Wilard. (2007). Thompson & Thompson Genetics in medicine. (7th edición). Saunders. ISBN 9781416030805.
- ↑ Alberts et al (2004). «Biología molecular de la célula». Barcelona: Omega. ISBN 54-282-1351-8.
- ↑ Kleinerman RA, Tucker MA, Tarone RE, et al. (abril de 2005). «Risk of new cancers after radiotherapy in long-term survivors of retinoblastoma: an extended follow-up». J. Clin. Oncol. 23 (10): 2272-9. PMID 15800318. doi:10.1200/JCO.2005.05.054.
- ↑ a b Gelehrter, T.; et al. (1998). Principles of Medical Genetics (2nd edición). Baltimore: Williams et Wilkins.
- ↑ Knudson AG (abril de 1971). «Mutation and cancer: statistical study of retinoblastoma». Proc. Natl. Acad. Sci. U.S.A. 68 (4): 820-3. PMC 389051. doi:10.1073/pnas.68.4.820.
- ↑ «The Evolution of Treatments for Retinoblastoma». Retina Today. Consultado el 29 de noviembre de 2011.
- ↑ «Superselective ophthalmic artery chemotherapy as primary treatment for retinoblastoma (chemosurgery». Ophtalmology. Consultado el 29 de noviembre de 2011.


 French
French Deutsch
Deutsch