Síndrome de ovario poliquístico , la enciclopedia libre
| Síndrome de ovario poliquístico | ||
|---|---|---|
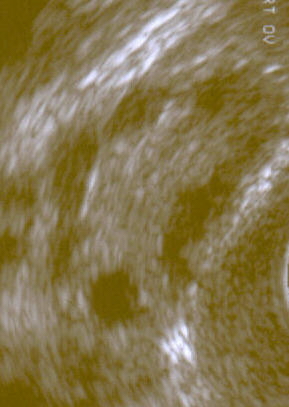 Ovario poliquístico en una imagen de ultrasonido | ||
| Especialidad | endocrinología ginecología | |
| Sinónimos | ||
| ||
El síndrome de ovario poliquístico (SOP), también llamado síndrome de Stein-Leventhal, es una enfermedad endocrina compleja y heterogénea que se caracteriza por alteraciones en el ciclo menstrual, fertilidad, hiperandrogenismo y ovario poliquístico. Generalmente esta causado por la producción anormal de testosterona y andrógenos, ambas hormonas masculinas. Un ovario se considera poliquístico cuando presenta 12 o más folículos antrales, y no porque el ovario tenga muchos quistes. El SOP es uno de los desequilibrios hormonales más frecuentes, y afecta entre un seis y un veinte por ciento de las mujeres en edad reproductiva, de acuerdo con el criterio diagnóstico que se ocupe. Su etiología es desconocida. No obstante, existe evidencia fuerte de que factores genéticos desempeñan un papel importante en su génesis.[1][2][3] [4][5][6]
El síndrome de ovario poliquístico no cursa con dolor, pero sí con dismenorrea (relación con la endometriosis). No es lo mismo ovario poliquístico (más de 12 folículos antrales detectados en ecografía) que síndrome de ovario poliquístico. Uno de los criterios para considerar síndrome de ovario poliquístico (SOP) es la presencia de más de 12 folículos antrales (ovarios poliquísticos), pero también anovulación/oligoovulación o hiperandrogenismo.[cita requerida]
Se considera que el síndrome de ovario poliquístico es una de las causas mayoritarias de la infertilidad femenina y el problema endocrino más frecuente en las mujeres en edad reproductiva.[1][7][8][9][10]
La gravedad de los síntomas varía de paciente a paciente. El diagnóstico debe descartar hiperplasia suprarrenal congénita, tumores que puedan secretar andrógenos y la hiperprolactinemia.[cita requerida]
Un estudio publicado en Nature Medicine encontró un vínculo entre el desequilibrio hormonal en el útero y síndrome de ovario poliquístico (SOP), específicamente exposición prenatal a hormona antimulleriana (AMH).[11] Para el estudio, los investigadores inyectaron ratonas embarazadas con AMH para que tuvieran una concentración de la hormona superior a la normal, que posteriormente dieron a luz a hijas que más tarde desarrollaron tendencias similares al síndrome de ovario poliquístico. Estos incluyen problemas con la fertilidad, la pubertad retrasada y la ovulación errática. Para revertirlo, los investigadores dosificaron las ratonas poliquísticas con cetrorelix, lo que hizo que los síntomas desaparecieran. Estos experimentos deberían confirmarse en humanos, pero podría ser el primer paso para comprender la relación entre el ovario poliquístico y la hormona antimulleriana.
Para diagnosticar el síndrome de ovario poliquístico deben darse 2 de los 3 criterios siguientes: presencia de ovario poliquístico en una ecografía, problemas de ovulación (anovulación/oligoovulación) y/o hiperandrogenismo. Por esta razón, es posible padecer SOP sin presentar ovario poliquístico per se; y al contrario, aunque la mayoría de las mujeres con SOP presentan ovario poliquístico, una mujer puede tener ovario poliquístico sin presentar el síndrome de ovario poliquístico.
Investigaciones recientes han arrojado luz sobre nuevas dimensiones del síndrome de ovario poliquístico (SOP), destacando avances significativos en la comprensión de sus mecanismos subyacentes. Estudios genéticos han identificado marcadores específicos relacionados con la predisposición genética al SOP, proporcionando una mayor claridad sobre las bases genéticas de la condición. Además, la investigación ha explorado vínculos más profundos entre el SOP y la salud metabólica, revelando conexiones con la resistencia a la insulina y el riesgo de diabetes tipo 2. Estos descubrimientos no solo mejoran nuestra comprensión de la complejidad del SOP, sino que también abren nuevas perspectivas para el desarrollo de terapias más específicas y personalizadas. A medida que la investigación progresa, se espera que estos avances contribuyan a la mejora de los enfoques diagnósticos y terapéuticos, brindando opciones más efectivas para quienes viven con esta condición.
Historia
[editar]En el año 1935 Stein y Leventhal describieron siete mujeres que sufrían amenorrea, hirsutismo, y ovarios agrandados con múltiples quistes.[3]
Cuadro clínico
[editar]Las pacientes presentan: oligoovulación o anovulación, que resulta en una menstruación irregular o amenorrea, infertilidad ligada a las alteraciones en la ovulación, y presencia de ovarios poliquísticos; exceso de actividad androgénica (esto es, de hormonas masculinizantes), lo que puede producir acné e hirsutismo; y resistencia a la insulina, generalmente asociada a la obesidad, diabetes tipo II e hipercolesterolemia.[12]
Los síntomas comunes del SOP incluyen:
- oligomenorrea y amenorrea (periodos menstruales irregulares, pocos o ausentes);[10][13]
- infertilidad, generalmente como consecuencia de la anovulación crónica (falta de ovulación);[13] además, estas mujeres tienen una incidencia superior de abortos espontáneos.
- acné e hirsutismo por exceso de hormonas masculinas ya que la deshidrosterona facilita la conversión del vello en pelos terminales en los folículos pilosos sensibles a andrógenos, así como hipermenorrea (menstruaciones frecuentes y abundantes);[10][14] aproximadamente tres cuartas partes de las pacientes presentan hiperandrogenemia;[15]
- síndrome metabólico, con tendencia a la obesidad central y otros síntomas relacionados con la resistencia a la insulina.[10] En concreto, la resistencia a la insulina aparece en el 80% de las mujeres que padecen este síndrome, siendo mayor el riesgo de desarrollo de diabetes mellitus tipo 2. Un síntoma clave del síndrome de ovario poliquístico es tener periodos menstruales irregulares o faltas de menstruación, ya que las consecuencias de esta afección sobre los ovarios pueden hacer que una joven deje de ovular. No obstante, puesto que una chica puede tardar hasta dos años en presentar períodos menstruales regulares desde su primera menstruación, cuesta mucho reconocer este síntoma de ovario poliquístico en las adolescentes. El desequilibrio hormonal que subyace a este síndrome puede desencadenar más cambios en el cuerpo de una chica, aparte de en los ovarios.
- Depresión
- Insomnio, muy relacionado con la resistencia a la insulina.
- Inflamación crónica, lo que puede afectar a la producción de óvulos y al sistema inmune, haciendo a las mujeres con SOP más sensibles a catarros, gripes o virus estomacales.
Por eso, los médicos se fijan en otros signos que también pueden indicar la presencia de un síndrome de ovario poliquístico:
Periodos muy fuertes o muy irregulares, incluso llegando a desaparecer por meses.
Aumento de peso, obesidad o dificultad para mantener un peso normal, especialmente cuando este peso de más se concentra alrededor de la cintura.
Una afección denominada hirsutismo,consistente en que las chicas tienen un exceso de vello en el rostro, pecho, abdomen, área del pezón o espalda (no obstante, tener un poco de vello en estas zonas es un rasgo completamente normal en algunas chicas).
Poco cabello en la cabeza (los médicos lo denominan alopecia).
Acné y poros obstruidos.
Oscurecimiento y engrosamiento de la piel alrededor de cuello, axilas o senos (afección denominada acantosis pigmentaria).
Hipertensión, colesterol alto o diabetes (concentración elevada de azúcar en sangre).
Las niñas que presentan en forma precoz determinados signos de la pubertad, como el desarrollo del vello púbico o axilar antes de los ocho años, tienen un riesgo incrementado de padecer un síndrome de ovario poliquístico más adelante.
Diagnóstico
[editar]Los criterios diagnósticos tanto del Instituto Nacional de Salud de Estados Unidos como de Róterdam establecen presentar algunas (mínimo dos) de las siguientes condiciones:[1][2]
- Hiperandrogenismo. Da lugar a unas manifestaciones cutáneas como son: acné, alopecia de patrón masculino e hirsutismo que se mide mediante la escala Ferriman-Gallwey que califica la presencia de vello en 9 áreas corporales.[16]
- Oligoovulación o anovulación. Se trata de problemas relacionados con la ovulación. El término oligoovulación hace referencia a un trastorno en el que se ovula pocas veces, pocos años, o en el que no se ovula con regularidad. Cuando, sin embargo, hablamos de anovulación nos referimos a ciclos en los que no se libera ningún óvulo. Entre los problemas asociados a la anovulación nos encontramos la falta de progesterona que si se suma a la presencia de muchos estrógenos (algo frecuente en los ovarios poliquísticos) conduce a un hiperestrogenismo no compensado. Este hiperestrogenismo no compensado produce un endometrio que prolifera de forma descontrolada, lo que puede dar lugar a un cáncer de endometrio. Por otro lado, al no tener progesterona para compensar el hiperestrogenismo, se puede generar un cáncer de mama.. La anovulación u oligoovulación se puede conocer según si la mujer tiene ciclos menstruales regulares o no. En el síndrome de ovario poliquístico es normal que se dé un largo tiempo sin tener la menstruación.
- Ecografía (prueba de imagen por ultrasonido) con alto número de folículos en los ovarios. Es necesaria la observación de más de 12 folículos antrales en la ecografía.
Cabe decir que una mujer puede tener síndrome de ovario poliquístico sin presentar en la ecografía ovarios poliquísticos, siempre que se cumplan los otros dos criterios.
En relación con el hiperestrogenismo, es una patología que per se sí es peligrosa, pero si está compensada con la progesterona no existiría tanto riesgo de contraer cáncer. Existen dos tipos de hiperestrogenismo: absoluto y relativo. En el absoluto se produce una excesiva cantidad de estrógenos que la progesterona no es capaz de compensar; en el relativo en cambio los niveles de estrógenos son normales, pero los de progesterona no son suficientes para compensarlos.
- Características morfológicas del ovario poliquístico: Es importante destacar que la presencia de ovario poliquístico no se requiere para establecer el diagnóstico de SOP. Por otro lado, la ecografía se debe hacer en la fase folicular temprana (día 3-5 del ciclo) para poder establecer el posible diagnóstico. La imagen debe mostrar la presencia de 12 o más folículos antrales de 2 a 9 mm de diámetro organizados en distribución periférica y central e incremento del estroma central mayor del 25% del área ovárica o un ovario con un volumen de más de 10 ml.
- Para el diagnóstico diferencial hay que descartar otras enfermedades que dar lugar a manifestaciones muy parecidas como son: hiperplasia suprarrenal congénita (HSC), neoplasias ováricas o suprarrenales, síndrome de Cushing, acromegalia, hiperprolactinemia, y otros como hipotiroidismo primario, obesidad y diabetes tipo 2 o falla ovárica prematura.[16]
Actualmente se ha observado que hay varios marcadores que si se miran en conjunto, pueden utilizarse para detectar el SOP. Éstas son la hormona anti-mulleriana, la LH, la proporción LH/FSH, además del íncide de masa corporal, así como otras características antropométricas. Se ha observado que da un valor extra al diagnóstico de esta enfermedad.[17]
Prevalencia y fenotipos
[editar]La prevalencia de SOP varía dependiendo del criterio de diagnóstico utilizado, fenotipos, así como de la población estudiada. El criterio de Róterdam tiene cuatro fenotipos:
| Fenotipo | |||
|---|---|---|---|
| A | Exceso de andrógenos | Disfunción ovulatoria | Morfología del ovario poliquístico |
| B | Exceso de andrógenos | Disfunción ovulatoria | - |
| C | Exceso de andrógenos | - | Morfología del ovario poliquístico |
| D | - | Disfunción ovulatoria | Morfología del ovario poliquístico |
Se considera que el fenotipo clásico son mujeres que presentan hiperandrogenismo y oligomenorrea con (A) o sin (B) morfología del ovario poloquístico cuando se les realiza una ecografía. En el fenotipo ovulatorio, las mujeres presentan hiperandrogenismo y morfología de ovario poliquístico (C). En el fenotipo no hiperandrogénico hay oligomenorrea y morfología del ovario poliquístico, sin hiperandrogenismo.
Se ha observado una prevalencia mayor de los fenotipos A y B en mujeres obesas, junto con resistencia a insulina así como un perfil cardiometabólico pobre. La prevalencia del síndrome metabólico era el menor en el fenotipo D. Sin embargo, estas diferencias son contradictorias en otros estudios, es por ello que es necesario una mayor investigación para que las guías de salud puedan definir mejor estos fenotipos y su relevancia clínica.
Tratamiento
[editar]El SOP (Síndrome del Ovario Poliquístico) es una patología muy habitual pero suele ser leve. Además, es una de las causas más frecuentes de infertilidad o disminución de la misma porque se ovula poco. Aun así, se suele resolver muy bien con los siguientes tratamientos. Si este no se trata en un extenso periodo de tiempo, pueden aumentar las posibilidades de padecer cáncer endometrial.
La acción terapéutica en el SOP dependerá del fenotipo, inquietudes y metas de la paciente. La terapia se centrará en:[18]
1) Suprimir y contrarrestar la secreción y acción de los andrógenos
2) Proteger al endometrio y corregir la disfunción menstrual
3) Mejorar el estado metabólico
4) Mejorar la fertilidad ovulatoria.
El modo de acción para conseguirlo en líneas generales será:
- Reducir el peso corporal, ya que de esta forma mejorarán, en el caso de que existieran: la diabetes, hipertensión y el colesterol alto mejorando la resistencia a insulina. El ejercicio regular puede ayudar, por tanto, a mejorar el peso además de que favorece el equilibrio de los niveles hormonales pues estimula la producción de endorfinas y reduce los niveles de adrenalina y cortisol (hormonas relacionadas con el estrés), así como reducir el riesgo a enfermedades cardiovasculares.
- El acné y el hirsurtismo responden bien a los antiandrogénicos.
- En aquellas mujeres en las que el tratamiento con anticonceptivos orales no esté contraindicado, deberá ser parte de la terapia inicial. Los anticonceptivos orales combinados inhiben la secreción de gonadotrofinas y la producción de andrógenos ováricos, regulan el sangrado vaginal y protegen el endometrio. Para las mujeres que tienen contraindicado los anticonceptivos se puede optar por anticonceptivos combinados transdérmicos o de progestina sola.
- Las mujeres que desean quedar embarazadas disponen de tratamientos hormonales especiales (citrato de clomifeno, gonadotropinas, metformina).
En caso contrario, se procede al tratamiento quirúrgico de los quistes.
- Modificación del estilo de vida principalmente.
- Farmacológico (antiandrógenos (espironolactona, finasterida, flutamida, ciproterona, dienogest), anticonceptivos hormonales, sensibilizadores de la insulina (metformina)][19]
Dentro del tratamiento farmacológico cabe destacar:
- Píldoras anticonceptivas combinadas. Se trata de píldoras que contienen tanto estrógenos como progesterona. Consiguen disminuir la producción de andrógenos y regulan los niveles de estrógenos. Regular las hormonas puede disminuir el riesgo de contraer cáncer de endometrio y corregir el sangrado anormal, el crecimiento excesivo de vello y el acné. Además de las píldoras anticonceptivas, pueden emplearse parches cutáneos o anillos vaginales que contienen la combinación de estrógenos y progesterona.
- Inositol, un suplemento alimenticio que puede ayudar a la eliminación de SOP lentamente de manera natural.[20]
Tratamiento nutricional
[editar]Hidratos de carbono
[editar]- Harinas integrales (avena, centeno, espelta)
- Pasta integral
- Arroz integral
- Legumbres, quinoa
- Copos de avena, muesli (sin azúcar)
Grasas
[editar]- Oliva, girasol, coco (natural)
- Frutos secos
- Semillas de linaza, semillas de calabaza
- Aguacates
- Mantequilla
Verduras
[editar]- Brócoli
- Espinacas
- Calabacines
- Judías verdes
Investigación
[editar]Recientemente se ha realizado una investigación sobre el SOP con un nuevo tratamiento, la naringenina. Para ello, indujeron SOP a una rata con sobrepeso a partir de letrozole. Con este tratamiento han observado una gran pérdida de peso en las ratas. Se cree que esta corrección tiene lugar en la etapa diestral, pues fue más prolongada en las ratas sometidas a tratamiento que a las que presentaban solo la enfermedad (las control). Además, se observó también una reducción del nivel de glucosa presente en plasma cuando se administraba naringenina. Por otro lado, a nivel hormonal también se reducía la cantidad de testosterona y estradiol presente en las ratas con SOP. En cuanto a la anatomía del ovario, las características propias de esta enfermedad (quistes, hiperplasias...), al suministrar naringenina disminuía notablemente.
Esto está demostrado tan solo en estudios animales, no obstante, si esta investigación sigue adelante y tiene unos efectos similares puede suponer un gran avance en el tratamiento de estos pacientes, pudiendo incluso tener descendencia.[21]
Referencias
[editar]- ↑ a b c Glintborg, Dorte; Andersen, Marianne (septiembre de 2016). «Management of endocrine disease: Morbidity in polycystic ovary syndrome» [Manejo de la enfermedad endocrina: morbilidad en el síndrome de ovario poliquístico]. Eur J Endocrinol (en inglés) (European Society of Endocrinology) 176: R53-R65. doi:10.1530/EJE-16-0373. Consultado el 11 de abril de 2017.
- ↑ a b McCartney, Christopher R.; Marshall, John C. (julio de 2016). «Polycystic ovary syndrome» [Síndrome de ovario poliquístico]. N Engl J Med (en inglés) 375 (1): 54-64. PMID 27406348. doi:10.1056/NEJMcp1514916. Consultado el 11 de abril de 2017.
- ↑ a b Sirmans, Susan M.; Pate, Kristen A. (diciembre de 2013). «Epidemiology, diagnosis, and management of polycystic ovary syndrome» [Epidemiología, diagnóstico y manejo del síndrome de ovario poloquístico]. Clin Epidemiol (en inglés) 6: 1-13. PMID 24379699. doi:10.2147/CLEP.S37559. Consultado el 11 de abril de 2017.
- ↑ Fauser, B. C. J. M.; Diedrich, K.; Bouchard, P.; Dominguez, F.; Matzuk, M.; Franks, S.; Hamamah, S.; Simon, C. et al. (2011). «Contemporary genetic technologies and female reproduction» [Tecnologías genéticas contemporáneas y reproducción femenina]. Human Reproduction Update 17 (6): 829-847. PMC 3191938. PMID 21896560. doi:10.1093/humupd/dmr033.
- ↑ Legro, R. S.; Strauss, J. F. (septiembre de 2002). «Molecular progress in infertility: polycystic ovary syndrome» [Progreso molecular en la infertilidad:síndrome de ovario poliquístico]. Fertility and Sterility 78 (3): 569-576. PMID 12215335. doi:10.1016/S0015-0282(02)03275-2.
- ↑ Diamanti-Kandarakis, E.; Kandarakis, H.; Legro, R. S. (agosto de 2006). «The role of genes and environment in the etiology of PCOS» [El rol de los genes y el ambiente en la etiología del SOP]. Endocrine 30 (1): 19-26. PMID 17185788. doi:10.1385/ENDO:30:1:19.
- ↑ Goldenberg, N.; Glueck, C. (2008). «Medical therapy in women with polycystic ovary syndrome before and during pregnancy and lactation» [Terapia médica en mujeres con síndrome de ovario poliquístico antes y durante el embarazo y lactancia]. Minerva Ginecol 60 (1): 63-75. PMID 18277353.
- ↑ Boomsma, C.M.; Fauser, B.C.; Macklon, N.S. (2008). «Pregnancy complications in women with polycystic ovary syndrome» [Complicaciones en el embarazo de mujeres con síndrome de ovario poliquístico]. Semin. Reprod. Med. 26 (1): 72-84. PMID 18181085. doi:10.1055/s-2007-992927.
- ↑ Azziz, R.; Woods, K.S.; Reyna, R.; Key, T. J.; Knochenhauer, E.S.; Yildiz, B. O. (junio de 2004). «The prevalence and features of the polycystic ovary syndrome in an unselected population» [La prevalencia y características del síndrome de ovario poliquístico en población no seleccionada]. Journal of Clinical Endocrinology & Metabolism 89 (6): 2745-9. PMID 15181052. doi:10.1210/jc.2003-032046.
- ↑ a b c d Teede, H.; Deeks, A.; Moran, L. (30 de junio de 2010). «Polycystic ovary syndrome: a complex condition with psychological, reproductive and metabolic manifestations that impacts on health across the lifespan» [Síndrome de ovario poliquístico: una condición compleja con manifestaciones psicológicas, reproductivas y metabólicas que impactan la salud a lo largo de la vida]. BMC Medicine (BioMedCentral) 8: 41. doi:10.1186/1741-7015-8-41. Consultado el 14 de noviembre de 2011.
- ↑ https://www.nature.com/articles/s41591-018-0035-5
- ↑ «Polycystic ovary syndrome».
- ↑ a b Mayo Clinic Staff (4 de abril de 2011). «Polycystic Ovary Syndrome – All». MayoClinic.com. Mayo Clinic. Consultado el 15 de noviembre de 2011.
- ↑ Christine Cortet-Rudelli, Didier Dewailly (21 de septiembre de 2006). «Diagnosis of Hyperandrogenism in Female Adolescents». Hyperandrogenism in Adolescent Girls. Armenian Health Network, Health.am. Consultado el 21 de noviembre de 2006.
- ↑ Huang A, Brennan K, Azziz R (abril de 2010). «Prevalence of hyperandrogenemia in the polycystic ovary syndrome diagnosed by the National Institutes of Health 1990 criteria». Fertil. Steril. 93 (6): 1938-41. PMC 2859983. PMID 19249030. doi:10.1016/j.fertnstert.2008.12.138.
- ↑ a b Builes, Carlos Alfonso; Díaz, Ivonne; Castañeda, Jimmy; Pérez, Luis Ernesto (2006). «Caracterización clínica y bioquímica de la mujer con Síndrome de Ovario Poliquístico». Revista Colombiana de Obstetricia y Ginecología (en inglés) 57 (1): 36-44. ISSN 2463-0225. Consultado el 12 de enero de 2020.
- ↑ Le, VNS; Le, DD; Nguyen, VQH; Chen, C; Cao, NT (2019). «Exploration of the role of anti‐Mullerian hormone and LH/FSH ratio in diagnosis of polycystic ovary syndrome». Clin. Endocrinol (Oxf). doi:10.1111/cen.13934.
- ↑ Fonseca Villanea, Carlos (1 de junio de 2018). «Síndrome de ovario poliquístico». Revista Medica Sinergia 3 (6): 9-15. ISSN 2215-5279. doi:10.31434/rms.v3i6.130. Consultado el 12 de enero de 2020.
- ↑ Este tratamiento se aplica antes de los 1o6 o 15 años de edad, pues en la mayoría de estos tratamientos se utilizan métodos anticonceptivos.
- ↑ Gomez, Dra. Cristina (27 de marzo de 2023). Que es el Inositol.
- ↑ Hong, Y; Yin, Y; Tan, Y; Hong, K; Zhou, H (2019). «The Flavanone, Naringenin, Modifies Antioxidant and Steroidogenic Enzyme Activity in a Rat Model of Letrozole-Induced Polycystic Ovary Syndrome». Med. Sci. Monit. 13 (25): 395-401. doi:10.12659/MSM.912341.


 French
French Deutsch
Deutsch