کرومات و دیکرومات - ویکیپدیا، دانشنامهٔ آزاد
| کرومات و دیکرومات | |||
|---|---|---|---|
| |||
| |||
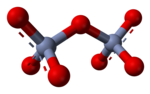
Chromate and dichromate | |||
| خصوصیات | |||
| فرمول مولکولی | CrO2- 4 و Cr 2O2- 7 | ||
| جرم مولی | 115.994 g mol-1 و 215.988 g mol-1 | ||
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |||
| Infobox references | |||
|
| |||
کرومات (به انگلیسی: Chromate) یک آنیون چند اتمی با فرمول شیمیاییCrO2−
4 و دی کرومات (به انگلیسی: dichromate) یک آنیون چند اتمی با فرمول شیمیایی Cr
2O2−
7 است. در این اکسیآنیونها اتم کروم در حالت اکسایش ۶+ میباشد. ترکیبات یونی حاوی این دو آنیون جز عوامل اکسید کننده نسبتاً قوی به شمار میروند. در محلولهای آبی، یون کرومات و دیکرومات میتوانند به صورت برگشت پذیر به هم ترادیسیده (تبدیل) شوند.
خواص شیمیایی
[ویرایش] کروماتها با هیدروژن پراکسید واکنش نشان میدهند و فرآوردههایی را میسازند که در آنها یون پراکسید(O2−
2) جایگزین یک یا چند اتم اکسیژن میشود. در محلول اسید، کمپلکس ناپایدار آبی پراوکسو کروم (VI) اکسید پراکسید، CrO(O2)2 ساخته میشود. این کمپلکس یک مولکول کووالانسی بی بار است، که ممکن است در اتر استخراج شود. با افزودن پیریدین، کمپلکس پایدارتر CrO(O2)2py شکل میگیرد.
خواص اسیدی-بازی
[ویرایش]در محلول آبی، آنیونهای کرومات و دیکرومات در تعادل شیمیایی میباشند.
- 2 CrO2−
4 + 2 H+ Cr
Cr
2O2−
7 + H2O
جستارهای وابسته
[ویرایش]منابع
[ویرایش]- Wikipedia contributors, "Chromate and dichromate," Wikipedia, The Free Encyclopedia, https://en.wikipedia.org/w/index.php?title=Chromate_and_dichromate&oldid=939501753 (accessed February 27, 2020).


 French
French Deutsch
Deutsch