Hémérythrine — Wikipédia
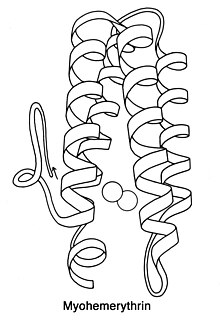
L'hémérythrine est une métalloprotéine oligomérique assurant le transport de l'oxygène O2 chez des invertébrés marins tels que les siponcles, les priapulides, les brachiopodes et chez un unique genre de polychètes, Magelona. La myohémérythrine est une métalloprotéine monomérique présente dans les muscles de ces invertébrés marins. Hémérythrine et myohémérythrine sont essentiellement incolores lorsqu'elles sont désoxygénées, et virent au rose violacé lorsqu'elles sont oxygénées.
Mécanisme de liaison à l'oxygène
[modifier | modifier le code]Le mécanisme de liaison de l'oxygène à cette protéine est inhabituel, et très différent de celui par exemple des hémoprotéines telles que l'hémoglobine ou la myoglobine. La plupart des transporteurs d'oxygène forment un ou plusieurs complexes métalliques entre un ou plusieurs groupes prosthétiques à métal de transition et une ou plusieurs molécules d'oxygène, tandis que l'hémérythrine transporte l'oxygène en formant un hydroperoxyde ROOH. Le site de liaison à l'oxygène consiste en une paire de cations de fer. Ceux-ci sont liés à la protéine à travers la chaîne latérale carboxylate de résidus de glutamate et d'aspartate ainsi qu'à travers cinq résidus d'histidine. L'hémérythrine et la myohémérythrine sont souvent décrites en fonction de l'état d'oxydation et de liaison de leurs cations de fer :
Fe2+–OH–Fe2+ désoxyhémérythrine (réduite) Fe2+–OH–Fe3+ semi-méthémérythrine Fe3+–O–Fe3+–OOH− oxyhémérythrine (oxydée) Fe3+–OH–Fe3+– (tout autre ligand) méthémérythrine (oxydée)
La liaison de l'oxygène à l'hémérythrine s'accompagne de l'oxydation à deux électrons des deux cations de fer ferreux Fe2+ pour donner deux cations de fer ferrique Fe3+ sont l'un est lié à un hydroperoxyde –OOH. Ce mécanisme est décrit par le schéma ci-dessous :
- Représentation de la liaison de l'oxygène O2 au site actif de l'hémérythrine.
L'un des deux cations ferreux est hexacoordonné tandis que l'autre est pentacoordonné. Ces deux cations sont liés par un hydroxyle formant un pont entre les deux. Une molécule d'oxygène s'insère entre l'atome d'hydrogène de cet hydroxyle et le cation ferreux pentacoordonné pour combler la position laissée vacante sur ce dernier, tandis que les cations ferreux sont oxydés en cations ferriques[1],[2].
Structure quaternaire et effet coopératif
[modifier | modifier le code]L'hémérythrine se présente typiquement sous forme d'homo-octamères et d'hétéro-octamères composés de sous-unités α et β de 13 à 14 kDa chacune, bien que certaines espèces aient des hémérythrines dimériques, trimériques et tétramériques. Chacune de ces sous-unités possède une structure formée de quatre hélices α qui se lie à la paire de cations ferreux. En raison de sa taille, l'hémérythrine est généralement présente dans des corpuscules ou des cellules du sang plutôt que flottant librement dans ce dernier.
Contrairement à l'hémoglobine, la plupart des hémérythrines sont dépourvues d'effet allostérique coopératif, ce qui réduit leur efficacité à environ le quart de celle de l'hémoglobine. Certains brachiopodes, en revanche, possèdent une hémérythrine qui présente un mécanisme de liaison à l'oxygène coopératif. Cet effet coopératif résulte d'interactions entre les sous-unités : la liaison d'une sous-unité à l'oxygène accroît l'affinité d'autres sous-unités pour l'oxygène.
L'affinité de l'hémérythrine pour le monoxyde de carbone CO est inférieure à son affinité pour l'oxygène, contrairement à ce qu'on observe pour l'hémoglobine, dont l'affinité pour le monoxyde de carbone est très élevée. Cette différence d'affinité résulte du mode de liaison de l'oxygène au groupe prosthétique de la protéine, qui est incompatible avec la liaison du monoxyde de carbone, lequel ne forme généralement pas de liaison hydrogène.
Domaine hémérythrine/HHE de liaison aux cations métalliques
[modifier | modifier le code]| Pfam | PF01814 |
|---|---|
| InterPro | IPR012312 |
| PROSITE | PDOC00476 |
| SCOP | 2hmq |
| SUPERFAMILY | 2hmq |
Le domaine hémérythrine/HHE est présent sous forme de domaine dupliqué des hémérythrines, des myohémérythrines et des protéines apparentées. Ce domaine se lie aux cations de fer dans l'hémérythrine, mais peut se lier à d'autres cations métalliques dans des protéines apparentées, comme le cadmium dans l'hémérythrine de Nereis diversicolor, de la famille des Nereididae. On le trouve également dans la protéine NorA de Cupriavidus necator, qui intervient dans la régulation de la réponse au monoxyde d'azote NO, ce qui suggère que ses ligands métalliques sont disposés différemment. Il existe également une autre protéine, chez Cryptococcus neoformans, qui possède un domaine hémérythrine/HHE et qui intervient dans la réponse au monoxyde d'azote[3]. Une protéine du staphylocoque doré qui contient ce domaine, la protéine SdcA de réparation des clusters fer-soufre, a été identifiée comme jouant un rôle important lorsque l'organisme bascule vers un environnement pauvre en oxygène : il est possible que cette protéine intervienne dans le stockage ou l'élimination de l'oxygène[4].
Notes et références
[modifier | modifier le code]- (en) D.M. Kurtz Jr., « 8.10 – Dioxygen-binding Proteins », Comprehensive Coordination Chemistry II, vol. 8, , p. 229-260 (DOI 10.1016/B0-08-043748-6/08171-8, lire en ligne)
- (en) Richard A. Friesner, Mu-Hyun Baik, Benjamin F. Gherman, Victor Guallar, Maria Wirstam, Robert B. Murphy et Stephen J. Lippard, « How iron-containing proteins control dioxygen chemistry: a detailed atomic level description via accurate quantum chemical and mixed quantum mechanics/molecular mechanics calculations », Coordination Chemistry Reviews, vol. 238-239, , p. 267-290 (DOI 10.1016/S0010-8545(02)00284-9, lire en ligne)
- (en) Eric D. Chow, Oliver W. Liu, Sean O’Brien et Hiten D. Madhani, « Exploration of whole-genome responses of the human AIDS-associated yeast pathogen Cryptococcus neoformans var grubii: nitric oxide stress and body temperature », 52, vol. 3, , p. 137-148 (PMID 17661046, DOI 10.1007/s00294-007-0147-9, lire en ligne)
- (en) Tim W. Overton, Marta C. Justino, Ying Li, Joana M. Baptista, Ana M. P. Melo, Jeffrey A. Cole et Lígia M. Saraiva, « Widespread Distribution in Pathogenic Bacteria of Di-Iron Proteins That Repair Oxidative and Nitrosative Damage to Iron-Sulfur Centers », Journal of Bacteriology, vol. 190, no 6, , p. 2004-2013 (PMID 18203837, DOI 10.1128/JB.01733-07, lire en ligne)


 French
French Deutsch
Deutsch