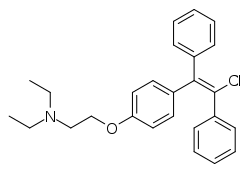
Clomifene
| Clomifene | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C26H28ClNO |
| Numero CAS | |
| Numero EINECS | 213-008-6 |
| Codice ATC | G03 |
| PubChem | 2800 |
| DrugBank | DBDB00882 |
| SMILES | CCN(CC)CCOC1=CC=C(C=C1)C(=C(C2=CC=CC=C2)Cl)C3=CC=CC=C3 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 | |
| attenzione | |
| Frasi H | 361 |
| Consigli P | 281 [1] |
Il clomifene rientra nella categoria dei modulatori selettivi del recettore degli estrogeni, uno dei principi attivi creati per contrastare gli effetti negativi degli estrogeni. Nel caso specifico il clomifene viene prevalentemente usato per trattare l'infertilità nelle donne che non ovulano.[2] Questo include il trattamento della sindrome dell'ovaio policistico.[2]
Nell'uomo viene utilizzato nella riduzione della ginecomastia.
L'utilizzo aumenta la possibilità di avere gemelli. È assunto per via orale una volta al giorno.[2]
Indicazioni cliniche
[modifica | modifica wikitesto]La FDA (Food and Drug Administration) ha approvato la somministrazione di clomifene come trattamento per:
- Infertilità anovulatoria o oligo-ovulatoria nelle donne (Induzione dell'ovulazione)
- Infertilità maschile (induzione della spermatogenesi)
Il clomifene, seppur non vi è alcuna approvazione da parte della FDA, viene anche utilizzato per il trattamento di:
- Ipogonadismo secondario
- Miglioramento delle prestazioni fisiche da parte di atleti sani, in quanto il clomifene induce un aumento dei livelli di testosterone
- Attacchi di cefalea nevralgiforme unilaterale di breve durata (SUNCT), una sotto forma di cefalee autonomiche trigeminali (TAC). [3]
Farmacologia
[modifica | modifica wikitesto]Clomifene è un SERM non steroideo che inibisce i recettori degli estrogeni nell'ipotalamo, inibendo così il feedback negativo degli estrogeni sul rilascio di gonadotropine (FSH e LH), portando all'up-regulation dell'asse ipotalamo-ipofisi-gonadico.[4]
Zuclomifene, un isomero più attivo, rimane legato per lunghi periodi di tempo.
Nel ciclo fisiologico femminile normale, a 7 giorni dall'ovulazione, alti livelli di estrogeno e progesterone prodotti dal corpo luteo inibiscono GnRH, FSH e LH all'ipotalamo e all'ipofisi anteriore. Se la fecondazione non si verifica nel periodo post-ovulazione il corpo luteo si disintegra a causa della mancanza di beta-hCG. Questo sarebbe normalmente prodotto dall'embrione nello sforzo di mantenere i livelli di progesterone e di estrogeni durante la gravidanza.
Dal punto di vista terapeutico, il clomifene viene somministrato all'inizio del ciclo mestruale. Generalmente viene prescritto a partire dal terzo giorno e continua per 5 giorni. A quel punto, il livello di FSH sta aumentando costantemente, causando lo sviluppo di alcuni follicoli. I follicoli a loro volta producono l'estrogeno, che circola nel siero. In presenza di clomifene, il corpo percepisce un basso livello di estrogeni, simile al giorno 22 nel ciclo precedente. Poiché l'estrogeno non può più esercitare un feedback negativo sull'ipotalamo, la secrezione di GnRH diventa più rapidamente pulsatile, il che si traduce in un aumento della gonadotropina ipofisaria (rilascio di FSH, LH).
Gli impulsi di ampiezza inferiore di GnRH e più rapidi portano ad una maggiore secrezione di LH / FSH, mentre gli impulsi di ampiezza più irregolari e più grandi di GnRH portano ad una diminuzione del rapporto di LH / FSH. Un aumento del livello di FSH causa la crescita di più follicoli ovarici, e successivamente rottura dei follicoli con conseguente ovulazione.
L'ovulazione si verifica più spesso 6-7 giorni dopo un ciclo di clomifene.
Il clomifene è anche usato negli uomini, come terapia off-label, nel trattamento dell'ipogonadismo maschile, non avendo, a differenza della terapia sostitutiva con testosterone, una soppressione della spermatogenesi ed altri possibili effetti collaterali.[5]
Farmacocinetica
[modifica | modifica wikitesto]Il clomifene viene somministrato per via orale e assorbito dal tratto gastrointestinale. La maggior parte del metabolismo del clomifene avviene nel fegato, dove subisce il ricircolo enteroepatico. Il clomifene e i suoi metaboliti sono escreti principalmente attraverso le feci (42%), ma anche attraverso le urine (8%) e l'escrezione può avvenire fino a 6 settimane dopo l'interruzione del farmaco.
L'elevata capacità di legame alle proteine plasmatiche, l'ingresso nel ciclo enteroepatico e l'accumulo nei tessuti adiposi aumentano l'emivita di eliminazione del CC che è di 5 giorni, sebbene se ne possano trovare tracce nelle feci fino a 6 settimane. E' importante ricordare che l'emivita (T/2) è il tempo necessario per diminuire la concentrazione plasmatica di un farmaco nell'organismo del 50%.
Farmacodinamica
[modifica | modifica wikitesto]Il Clomifene è in grado competere con l'estradiolo e interagire con i tessuti contenenti recettori per gli estrogeni, inclusi l'ipotalamo, l'ipofisi, l'ovaio, l'endometrio, la vagina e la cervice. Agendo come un anti-estrogeno sul sistema nervoso centrale, il clomifene si lega ai recettori per gli estrogeni (ERs) presenti nell'ipotalamo per periodi prolungati, bloccando funzionalmente il feedback negativo generato dall'estradiolo nei confronti dell'ipotalamo e dell'ipofisi.[6] Questo effetto aumenta la secrezione dell'ormone di rilascio delle gonadotropine (GnRH) da parte dell'ipotalamo nelle donne con problemi di anovulazione.
L'aumento della pulsatilità del GnRH determina un aumento della secrezione delle gonadotropine FSH (ormone follicolo-stimolante) e LH (ormone luteinizzante) dall'adenoipofisi. Le gonadotropine, dopo essere state rilasciate dalla ghiandola pituitaria, sono in grado di avviare il corretto processo di crescita follicolare a livello ovarico, fino alla rottura follicolare che determina l'ovulazione.
La somministrazione di clomifene in pazienti anovulatorie è accompagnata da un aumento del 50% dell'FSH endogeno, un tasso di ovulazione del 60-90% e un tasso di gravidanza del 30-40%.
Attraverso lo stesso meccanismo presente nelle donne, il clomifene è in grado di bloccare il feedback negativo esercitato dall'estradiolo nei confronti dell'ipotalamo e dell'ipofisi, dunque indurre la secrezione di GnRH dall'ipotalamo e di LH dall'adenoipofisi, negli uomini. L'ormone luteinizzante, negli uomini, agisce a livello dei testicoli determinando la sintesi di testosterone da parte delle cellule di Leydig. Questo processo è necessario per indurre la spermatogenesi in uomini che hanno problemi di fertilità.
Controindicazioni
[modifica | modifica wikitesto]Sconsigliato in soggetti con insufficienza e malattie a livello epatico, da evitare in caso di gravidanza essendo tale lo scopo della terapia.
Risulta assolutamente controindicato se vi è presenza di fibroma uterino. Se nel corso del trattamento compaiono dei disturbi visivi bisogna immediatamente cessare la somministrazione del farmaco e ricorrere ad un oculista.
Effetti indesiderati
[modifica | modifica wikitesto]Fra gli effetti indesiderati si riscontrano depressione, vampate, perdita di capelli, insonnia, cefalea, nausea, rash cutaneo, aumento di peso, convulsioni, dolore addominale, menorragia, endometriosi.
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. dell'11.10.2012, riferita al citrato
- ^ a b c "Clomiphene Citrate". The American Society of Health-System Pharmacists..
- ^ Marilyn K. Mbi Feh e Roopma Wadhwa, Clomiphene, StatPearls Publishing, 2021. URL consultato il 5 gennaio 2022.
- ^ Clomifene.
- ^ Lorenzo DiGiorgio e Hossein Sadeghi-Nejad, Off label therapies for testosterone replacement, in Translational Andrology and Urology, vol. 5, n. 6, 2016-12, pp. 844–849, DOI:10.21037/tau.2016.08.15. URL consultato il 7 febbraio 2019.
- ^ CLOMIPHENE CITRATE, su dailymed.nlm.nih.gov. URL consultato il 5 gennaio 2022.
Bibliografia
[modifica | modifica wikitesto]- British national formulary, Guida all’uso dei farmaci 4 edizione, Lavis, agenzia italiana del farmaco, 2007.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su clomifene
Wikimedia Commons contiene immagini o altri file su clomifene
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) clomiphene, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.


 French
French Deutsch
Deutsch