Kalciumfluorid – Wikipedia
| Kalciumfluorid | |
 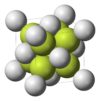 | |
| Systematiskt namn | Kalciumfluorid |
|---|---|
| Övriga namn | Fluorit |
| Kemisk formel | CaF2 |
| Molmassa | 78,07 g/mol |
| Utseende | Vita kristaller |
| CAS-nummer | 7789-75-5 |
| SMILES | [Ca+2].[F-].[F-] |
| Egenskaper | |
| Densitet | 3,18 g/cm³ |
| Löslighet (vatten) | 0,016 g/l (20 °C) |
| Smältpunkt | 1418 °C |
| Kokpunkt | 2533 °C |
| Faror | |
| Huvudfara | Inga |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Kalciumfluorid är en kemisk förening av kalcium och fluor. Den förekommer naturligt som mineralet fluorit och är råmaterial för huvuddelen av världens fluorföreningar. Det är ett salt som är svårlösligt i vatten. Rena kristaller är färglösa, men föroreningar av rent kalcium, fluor eller elektronfyllda hål i kristaller (F-centra) kan ge olika färger.
Användning
[redigera | redigera wikitext]Framställning av vätefluoriid
[redigera | redigera wikitext]Vätefluorid är den syra som bildar fluorider. Eftersom den är såpass hälsofarlig så tillverkas den oftast på plats genom att låta svavelsyra reagera med kalciumfluorid.
Andra applikationer
[redigera | redigera wikitext]Kristall av kalciumfluorid är transparent för ljus inom spektrumet med våglängden 0,15–9 μm, vilket inkluderar både ultraviolett och infrarött såväl som synligt ljus (0,38–0,74 μm). Dessutom har det lågt brytningsindex vilket gör det lämpligt för optiska tillämpningar.
Uran-dopad kalciumfluorid användes i en av de första lasrarna.


 French
French Deutsch
Deutsch
