Hidrasyon - Vikipedi
Endüstride küçük moleküllü alkollerin elde edilmesi için kullanılan bir yöntemdir. Bu yöntem alkenlerin hidrasyonu olarak da adlandırılmaktadır. Su kötü bir nüklefil olduğu için genellikle alkenlerle su katma tepkimeleri istenilen ürünü yani alkolleri vermezler. Bu yüzden bu tepkimeler çoğunlukla bir asit katalizörün varlığında gerçekleştirilir. Sülfürik asit ve fosforik asit alkenlerin hidrasyonu esnasında en sık kullanılan asitlerdir. Hidrasyon tepkimeleri genel itibarıyla Markownikow-Kuralı çerçevesinde gerçekleşen bir tepkimedir.[1]
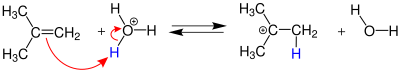
Alkenlere su katılmasında tepkimenin hızını belirleyen kısım 1.basamaktır ve diğer iki basamaktadan oldukça yavaş gerçekleşir. Diğer bir deyişle karbokatyon oluşumu, tepkimenin hızını belirten aşamadır. Bu basamakta öncelikli oluşan karbokatyon üçüncül karbokatyonudur. Çünkü üçüncül karbokatyon birincile göre daha kararlıdır. Bu basamakta diğer önemli bir olayda alkenin yapısına katılan hidrojenin asit katalizörden koparılmasıdır. Bu basamağın sonunda bir molekül su ve ara ürün olan üçüncül bir karbokatyon oluşmaktadır.[2]
İkinci basamak ise ilk basamakta oluşan karbokatyonun yapısına bir su molekülün eklenmesiyle protonlanmış bir olkol oluşmaktadır. Son olarak ikinci aşamanın sonunda oluşan protonlanmış alkolden bir proton ortamdaki bir su molekülüne aktarılarak ter-bütil alkol katalizörümüz olan asit oluşmaktadır.[3]
Kaynakça
[değiştir | kaynağı değiştir]- T.W Graham Solamons(Yazar), Craig B. Fryhle (Yazar),Güral Okay (Çeviri Editörü), Yılmaz Yıldırır (Çeviri Editörü) Organik Kimya, (Organik Chemsty), 7. Basımdan Çeviri, Literatür Yayıncılık 2002, ISBN 975-8431-87-0. Sayfa 331-334
- ^ T.W Graham Solamons( Yazar), Craig B. Fryhle (Yazar),Güral Okay (Çeviri Editörü), Yılmaz Yıldırır (Çeviri Editörü) Organik Kimya, ( Organik Chemsty), 7. Basımdan Çeviri, Literatür Yayıncılık 2002, ISBN 975-8431-87-0 sayfa 331
- ^ T.W Graham Solamons( Yazar), Craig B. Fryhle (Yazar),Güral Okay (Çeviri Editörü), Yılmaz Yıldırır (Çeviri Editörü) Organik Kimya, ( Organik Chemsty), 7. Basımdan Çeviri, Literatür Yayıncılık 2002, ISBN 975-8431-87-0 sayfa 332-333
- ^ T.W Graham Solamons( Yazar), Craig B. Fryhle (Yazar),Güral Okay (Çeviri Editörü), Yılmaz Yıldırır (Çeviri Editörü) Organik Kimya, ( Organik Chemsty), 7. Basımdan Çeviri, Literatür Yayıncılık 2002, ISBN 975-8431-87-0 sayfa 334


 French
French Deutsch
Deutsch